O QUE É CBG?
O canabigerol (CBG) é um dos principais fitocanabinoides presentes na cannabis sativa L., possível resultado da degradação do ácido canabigerólico (CBGA), o principal precursor de vários canabinoides.
O crescente interesse pelo CBG tem sido atribuído às suas propriedades não psicotrópicas, baixa potência do receptor canabinoide e abundância relativa em algumas variedades comerciais de Cannabis. No campo terapêutico, foi descrito um amplo perfil farmacológico, onde o CBG apresenta propriedades anti-inflamatórias, anticancerígenas, antioxidantes, antimicrobianas, neuroprotetores, estimuladoras do apetite, dentre outras. Revisões anteriores sobre o CBG limitavam-se ao potencial farmacológico da molécula, com poucos detalhes sobre a química, ou aos avanços nas ferramentas analíticas usadas para explorar o conteúdo do CBG.
Sabe-se que o cannabigerol está presente nos tricomas (pequenos crescimentos da planta) na forma de ácido (CBGA) e é o primeiro a se desenvolver na planta de cannabis: por isso, como dito acima, é considerado o precursor dos ácidos mais comuns, que compõem CBD e THC. Após a colheita, as plantas que contêm os fitocanabinoides são secas e processadas e, graças ao calor utilizado nessas etapas, os componentes perdem suas características ácidas, com a remoção de um grupo carboxila. Graças a esse processo, que é chamado de “descarboxilação”, os ácidos são transformados em seus equivalentes não ácidos, como THC, CBD e CBG. Durante a floração, o canabinóide mais abundante é o CBG, mas quando a substância é seca, sua concentração geralmente é inferior a 1% (um por cento). Por esse motivo, o composto não recebeu atenção especial dos estudiosos nos últimos anos.
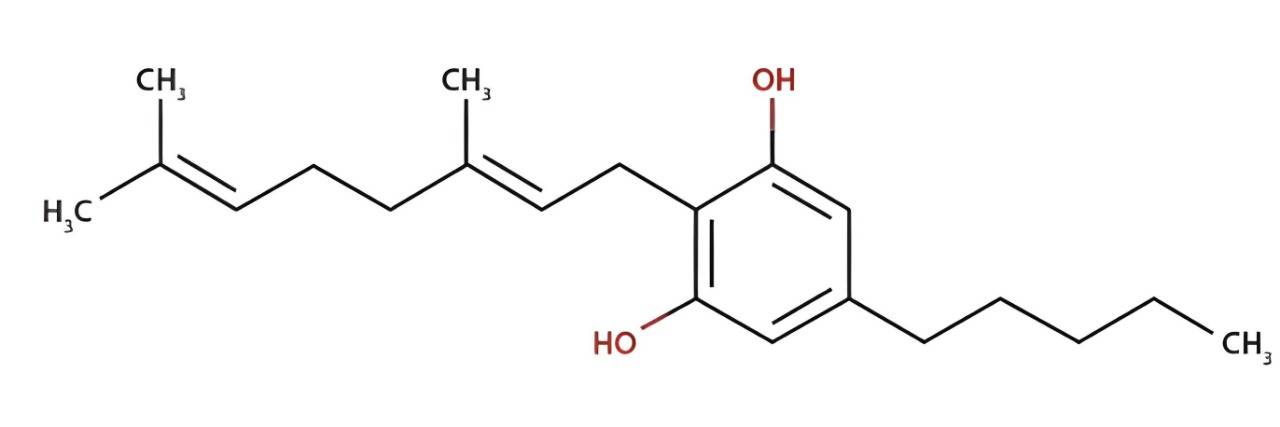
Fórmula Molecular C21H32O2
Dos estudos concluídos, a vasta maioria são conduzidos in vitro ou utilizando modelos animais. Todavia, ainda assim fornecem um forte indicador do potencial terapêutico do CBG.
O CBG não está contido na Convenção das Nações Unidas sobre Substâncias Psicotrópicas, razão pela qual este fitocanabinoides e seus derivados são legais na maioria dos países.
Graças ao conhecimento técnico e equipamentos de última geração utilizados para produzir os extratos da VALTELLINAMED, a nossa fórmula tradicional de espetro integral (Full Spectrum) possui quantidades padronizadas de CBG, fornecendo assim o máximo potencial do canabinoide em benefício do bem-estar.
O POTENCIAL DO CBG
Estudos realizados décadas atrás mostraram a capacidade inibitória na absorção do ácido aminobutírico (GABA), com consequentes atividades relaxantes: por isso, o CBG poderia ser útil também no tratamento da ansiedade e da tensão muscular. Outras pesquisas que datam da segunda metade dos anos 1900 destacaram os efeitos analgésicos e antifúngicos do canabigerol.
Mais recentemente, o CBG demonstrou ser potencialmente eficaz contra o câncer de mama, pele e próstata. Além disso, o fitocanabinoide pode representar um auxílio contra a psoríase, pois inibe a proliferação de queratinócitos. Outros usos potenciais do CBG foram identificados no tratamento do glaucoma, pois reduz a pressão intraocular e no tratamento de doenças inflamatórias intestinais, disfunção da bexiga e pode ser uma solução promissora como antidepressivo ou antiemético.
Nos últimos anos foram publicados diversos estudos sobre a farmacologia da CBG e suas potenciais aplicações médicas. A literatura destaca suas inúmeras propriedades farmacológicas que vão desde ações adrenérgicas, serotoninérgicas, canabinérgicas e transitórias do potencial receptor (TRP), até a modulação de enzimas, como ciclooxygenase, a lipase de monoacilglicerol (também conhecida como lipase MAG, acilglicerol lipase, MAGL, MGL ou MGLL), N-acylethanolamina amidase (NAAA) e fosfolipase-A2 (PLA2).
Possíveis aplicações médicas do CBG foram alvo de diversas publicações científicas, algumas das quais inspiraram o início de patentes para proteger seus usos terapêuticos. A literatura atual oferece evidências de seus potenciais como um agente anti-inflamatório e anticancerígeno, para citar apenas alguns, abordando o interesse neste fitocanabinoide como um potencial material inicial para novos agentes terapêuticos.
Pesquisas nas últimas décadas também têm investigado amplamente as propriedades antioxidantes dos produtos naturais como uma abordagem terapêutica para a prevenção e o tratamento de distúrbios relacionados ao estresse oxidativo. Nesse contexto, diversos estudos tiveram como objetivo avaliar o potencial terapêutico dos fitocanabinoides, os compostos bioativos da Cannabis sativa, principalmente a capacidade antioxidante do Canabigerol (CBG). Tais resultados, embora ainda in vitro, mostraram que a CBG é capaz de neutralizar o estresse oxidativo pela ativação dos receptores CB2. Especificamente, a CBG apresentou uma ação potente na inibição do estresse oxidativo, pela redução da regulação dos principais marcadores oxidativos (iNOS, nitrotyrosina e PARP-1), impedindo a α fosforilação e translocação do fator nuclear -κB (NF-κB) e também através da modulação da via de análises de kmófas MAP.
Assim, com base em suas atividades antioxidantes, a CBG pode ser uma grande promessa como um agente antioxidante e, portanto, usada na prática clínica como uma nova abordagem em distúrbios relacionados ao estresse oxidativo.
Está interessado em explorar o potencial terapêutico do CBG? Conheça nosso catálogo para consultar uma gama completa de produtos de espetro integral (Full Spectrum).
Referências:
Giacoppo S, Gugliandolo A, Trubiani O, et al. Os receptores cb2 canabinóides estão envolvidos na proteção de macrófagos RAW264.7 contra o estresse oxidativo: um estudo in vitro. Eur J Histochem. 2017;61(1):2749. Publicado em 2017 Jan 23. doi:10.4081/ejh.2017.2749.
ACS Infect. Dis. 2020, 6, 3, 338–346. Publication Date:February 4, 2020 https://doi.org/10.1021/acsinfecdis.9b00419. Copyright © 2020 American Chemical Society.
Potential Clinical Uses of CBG. Rahul Nachnani, Wesley M. Raup-Konsavage and Kent E. Vrana. Journal of Pharmacology and Experimental Therapeutics February 1, 2021, 376 (2) 204-212; DOI: https://doi.org/10.1124/jpet.120.000340.
Nicholas G. Jentsch, Xiong Zhang, Jakob Magolan. Efficient Synthesis of Cannabigerol, Grifolin, and Piperogalin via Alumina-Promoted Allylation. Journal of Natural Products 2020, 83 (9), 2587-2591. https://doi.org/10.1021/acs.jnatprod.0c00131.
Chinedu P. Anokwuru, Felix L. Makolo, Maxleene Sandasi, Sidonie Y. Tankeu, Ishaku L. Elisha, Clement Agoni, Sandra Combrinck, Alvaro Viljoen. Cannabigerol: a bibliometric overview and review of research on an important phytocannabinoid. Phytochemistry Reviews 2022, 406 https://doi.org/10.1007/s11101-021-09794-w.
Muna Aqawi, Ronit Vogt Sionov, Ruth Gallily, Michael Friedman, Doron Steinberg. Anti-Biofilm Activity of Cannabigerol against Streptococcus mutans. Microorganisms 2021, 9 (10), 2031. https://doi.org/10.3390/microorganisms9102031.
Rahul Nachnani, Wesley M. Raup-Konsavage, Kent E. Vrana. The Pharmacological Case for Cannabigerol. Journal of Pharmacology and Experimental Therapeutics 2021, 376 (2), 204-212. https://doi.org/10.1124/jpet.120.000340.
Navarro G, Varani K, Reyes-Resina I, et al. Cannabigerol action at cannabinoid CB1 and CB2 receptors and at CB1-CB2 heteroreceptor complexes. Front Pharmacol 2018;9:632.
Borrelli F, Pagano E, Romano B, et al. Colon carcinogenesis is inhibited by the TRPM8 antagonist cannabigerol, a cannabis-derived non-psychotropic cannabinoid. Carcinogenesis 2014;35(12):2787-97.
Baek SH, Kim YO, Kwag JS, et al. Boron trifluroide etherate on silica-A modified Lewis acid regent (VII). Anti-tumor activity of cannabigerol against human oral epitheloid carcinoma cells. Arch Pharm Res 1998;21(3):353-6.
Brierley DI, Samuels J, Duncan M, et al. A cannabigerol-rich Cannabis sativa extract, devoid of [increment] 9-tetrahydrocannabinol, elicits hyperphagia in rats. Behav Pharmacol 2017;28(4): 280-4.
Brierley DI, Harman JR, Giallourou N, et al. Chemotherapy-induced cachexia dysregulates hypothalamic and systemic lipoamines and is attenuated by cannabigerol. J Cachexia Sarcopenia Muscle 2019.
Aguareles J, Paraiso-Luna J, Palomares B, et al. Oral administration of the cannabigerol derivative XCE-003.2 promotes subventricular zone neurogenesis and protects against mutant huntingtin-induced neurodegeneration. Transl Neurodegener 2019; 8:9.
Rodriguez-Cueto C, Santos-Garcia I, Garcia-Toscano L, et al. Neuroprotective effects of the cannabigerol quinone derivative VCE-003.2 in SOD 1-G93A transgenic mice, an experimental model of amyotrophic lateral sclerosis. Biochem Pharmacol 2018; 157:217-226.
Garcia C, Gomez-Canas M, Burgaz S, et al. Benefits of VCE-003.2, a cannabigerol quinone derivative, against inflammation-driven neuronal deterioration in experiemental Parkinson’s disease:possible involvement of different binding sites at the PPARg receptor. J Neuroinflammation 2018;15(1):19.
Pagano E, Montanaro V, Di Girolamo A, et al. Effect of non-psychotropic plant-derived cannabinoids on bladder contractility:focus on cannabigerol. Nat Prod Commun 2015;10(6):1009-12.



